Общая химия/Классификация материи
Классификация материи
Материю можно классифицировать по ее состоянию.
- Твердые тела имеют фиксированный объем и форму. Межмолекулярная сила притяжения для твердого вещества очень сильна.
- Жидкости имеют фиксированный объем, но меняют форму. Межмолекулярная сила притяжения для жидкого вещества слабее, чем для твердого вещества.
- Газы не имеют ни определенного объема, ни формы. Межмолекулярная сила притяжения для газообразного вещества пренебрежимо мала.
- Плазма, которая обычно является газообразным состоянием вещества, в котором часть или все атомы или молекулы диссоциируют с образованием ионов.
- Конденсат Эйнштейна-Бозе (EBC) - это теоретическое состояние вещества. Межмолекулярная сила притяжения для EBC настолько сильна, что молекулы вообще не могут двигаться.
Материю также можно классифицировать по ее химическому составу.
- элемент — это чистое вещество, состоящее из атомов с одинаковым числом протонов. По состоянию на 2011 год было обнаружено 118 элементов, 92 из которых встречаются в природе. Углерод (C), Кислород (O), Водород (H) — примеры элементов. периодическая таблица — это табличное представление известных элементов.
- соединение состоит из двух или более химических элементов, которые химически связаны друг с другом. Вода (H2O) и столовый сахар (C12H22O11) — примеры химических соединений. Соотношение элементов в соединении всегда одинаково. Например, в воде число атомов H всегда в два раза больше числа атомов O.
- смесь состоит из двух или более веществ (элементов или соединений), смешанных вместе без какой-либо химической связи. Салат является хорошим примером. Смесь может быть разделена на отдельные компоненты механическими средствами.
Типы смесей
Существует много видов смесей. Они классифицируются по поведению фаз или смешанных веществ.
Гомогенные смеси

Гомогенная смесь является однородной, что означает, что любой данный образец смеси будет иметь тот же состав. Воздух, морская вода и углекислый газ, растворенный в газировке, являются примерами гомогенных смесей или растворов. Независимо от того, какой образец вы возьмете из смеси, он всегда будет состоять из той же комбинации фаз. Шоколадное мороженое неоднородно — в одной ложке может быть две крошки, а в другой — несколько.
Примером однородной смеси является раствор. Растворяющееся вещество — это «растворенное вещество». Растворяющее вещество — это «растворитель». Вместе они образуют «раствор». Если размешать ложку соли в стакане воды, соль — это растворяющееся вещество. Вода — это растворитель. Соленая вода теперь является раствором или однородной смесью соли и воды.
Когда смешиваются разные газы, они всегда образуют раствор. Молекулы газа быстро распределяются в однородную композицию.
Гетерогенные смеси
Гетерогенная смесь' неоднородна. Разные образцы могут иметь разный состав, как, например, мороженое с шоколадной крошкой. Бетон, почва, кровь и салат — все это примеры гетерогенных смесей.

Суспензии
Когда песок поднимается в пруду, он замутняет воду. Он имеет большую массу, чем вода, поэтому он опускается на дно и оседает, и больше не смешивается с водой. Это пример суспензии. Суспензии — это гетерогенные смеси, которые в конечном итоге оседают. Они обычно, но не обязательно, состоят из фаз в разных состояниях вещества. Итальянская заправка для салата состоит из трех фаз: воды, масла и мелких кусочков приправы. Приправы — это твердые вещества, которые опустятся на дно, а масло и вода — это жидкости, которые разделятся.
Коллоиды

Что такое зубная паста? Мы не можем точно классифицировать ее по состоянию вещества. Она имеет определенную форму и объем, как твердое тело. Но когда вы сжимаете тюбик, она течет почти как жидкость. А еще есть желе, крем для бритья, дым, тесто и Silly Putty...
Это примеры коллоидов. коллоид — это гетерогенная смесь двух веществ в разных фазах. Крем для бритья и другие пены — это газ, диспергированный в жидкости. Желе, зубная паста и другие гели — это жидкость, диспергированная в твердом теле. Тесто — это твердое вещество, диспергированное в жидкости. Дым — это твердое вещество, диспергированное в газе.
Шаблон:Информация
Коллоиды состоят из двух фаз: «дисперсная фаза» внутри «сплошной среды».
Эффект Тиндаля
Эффект Тиндаля отличает коллоиды от растворов. В растворе частицы настолько малы, что не рассеивают свет. Это не относится к коллоидам. Если вы прольете свет через раствор, луч света не будет виден. Он будет виден в коллоиде. Например, если вы когда-либо играли с лазерной указкой, вы видели эффект Тиндаля. Вы не можете увидеть лазерный луч в воздухе (растворе), но если вы направите его в туман, луч будет виден. Облака выглядят белыми (или серыми), а не синими, из-за эффекта Тиндаля — свет рассеивается мелкими каплями взвешенной воды.
Методы разделения смесей
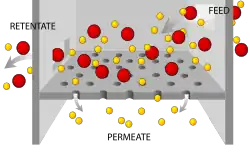
Поскольку в смеси нет химических связей, фазы можно разделить механическими средствами. В гетерогенной смеси, такой как салат, кусочки можно легко выбрать и разделить. Это так же просто, как просеять салат и выбрать все помидоры и редиски, например. Однако многие смеси содержат частицы, которые слишком малы, жидкости или слишком много частиц, чтобы их можно было разделить вручную. Мы должны использовать более сложные методы для разделения смеси.
Фильтрация
Представьте, что у вас есть песочница, но в ней есть кусочки битого стекла. Все, что вам нужно, — это какой-то фильтр. Частицы песка намного меньше стеклянной крошки, поэтому сетчатый фильтр пропустит песок, но задержит стекло. Фильтрация используется во всех видах методов очистки. Некоторые фильтры, например, диализные трубки, настолько тонкие, что пропускают воду, но не растворенную глюкозу.
Шаблон:Информация
Дистилляция
Если бы вам дали стакан соленой воды, вы бы смогли ее выпить? Конечно, если бы вы сначала ее дистиллировали. Дистилляция — это кипячение смеси для разделения ее фаз. Соль — твердое вещество при комнатной температуре, а вода — жидкость. Вода закипит задолго до того, как соль начнет плавиться. Поэтому разделить их так же просто, как кипятить воду до тех пор, пока не останется только твердая соль. При желании водяной пар можно собрать, сконденсировать и использовать в качестве источника чистой воды.
Дистилляция также может быть использована, если две жидкости смешаны, но имеют разные точки кипения. Разделение нескольких жидкостей с близкими точками кипения может быть достигнуто с помощью фракционирования.
Центрифугирование и осаждение
Эти процессы основаны на разнице в плотности. В медицинской лаборатории кровь часто попадает в центрифугу. Центрифуга — это машина, которая вращает образец с довольно высокой скоростью. Эритроциты намного плотнее водянистого вещества (называемого плазмой, но это не плазменное состояние вещества), из которого состоит кровь. В результате вращения более плотные фазы перемещаются наружу, а менее плотные фазы перемещаются внутрь, по направлению к оси вращения. Затем эритроциты можно отделить от плазмы.
Осаждание похоже, но оно происходит, когда частицы разной плотности оседают в жидкости. Если оставить банку с мутной водой отстаиваться, то самые тяжелые частицы опустятся на дно первыми. Самые легкие частицы опустятся последними и образуют слой поверх более тяжелых частиц. Вы могли видеть этот эффект в бутылке с заправкой для салата. Приправы опускаются на дно, вода образует нижний слой, а масло — верхний. Отдельные фазы можно снять. Чтобы вернуть смесь, просто встряхните ее, чтобы нарушить слои.
Уникальные свойства
Различия в свойствах веществ можно использовать для разделения. Рассмотрим следующие примеры:
- Смесь песка и железных опилок можно разделить с помощью магнита.
- Соль и песок можно разделить раствором (песок не растворится в воде, соль растворится)
- Гелий можно отделить от смеси с водородом путем сжигания (это очень опасная операция, так как водород в присутствии кислорода очень взрывоопасен). Водород горюч, а гелий — нет.
Другие методы
Существует бесчисленное множество других способов разделения смесей. Например, гель-электрофорез используется для разделения фрагментов ДНК разного размера. Их помещают в гель и пропускают электрический ток. Меньшие фрагменты движутся быстрее и отделяются от больших.
Хроматография разделяет фазы, растворенные в жидкости. Если вы хотите увидеть пример, возьмите полоску бумаги и нарисуйте на ней точку цветным маркером. Окуните полоску в воду и подождите некоторое время. Вы должны увидеть, как чернила разделяются на разные цвета, растекаясь от точки.